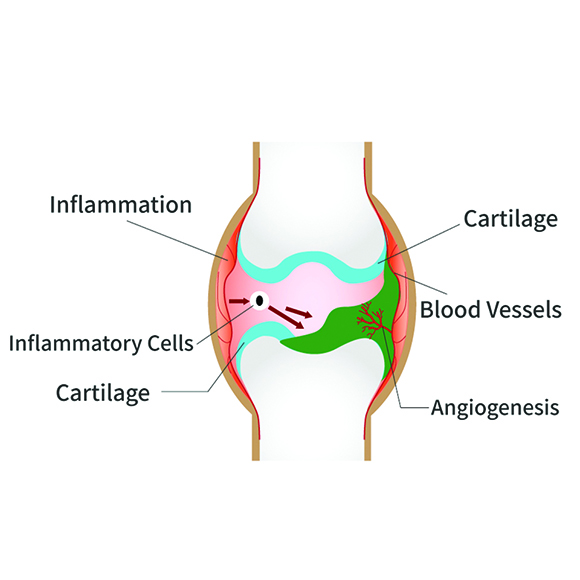
มาโคลิปิน (ลิปิดสกัดจากปลาฉลาม) คือ ลิปิดเข้มข้นที่สกัดออกมาได้จากเนื้อปลาฉลาม มาโคลิปินมีคุณสมบัติชั้นเลิศในการยับยั้งกระบวนการ Angiogenesis หรือการสร้างเส้นเลือดใหม่ซึ่งเป็นกุญแจสู่การยับยั้งการเจริญเติบโตเนื้องอกและการแพร่กระจายของมะเร็ง อีกทั้งยังเป็นประโยชน์ต่อโรคที่เกี่ยวข้องกับการงอกของเส้นเลือดใหม่ ซึ่งรวมถึงเมตาบอลิกซินโดรม โรคสะเก็ดเงิน โรคไขข้ออักเสบรูมาตอยด์ โรคจอประสาทตาเสื่อม โรคจอตาเสื่อมจากเบาหวาน และความผิดปกติของผิวหนังสืบเนื่องจากวัย Angiogenesis หมายถึงการมีเส้นเลือดงอกใหม่ขึ้น แม้ว่าการสร้างเส้นเลือดใหม่จะเป็นการทำงานที่สำคัญอย่างหนึ่งทางสรีรวิทยาและการเจริญเติบโตตามปกติของร่างกาย แต่เมื่อเกี่ยวข้องกับมะเร็งและโรคภัยอื่นๆแล้ว การงอกใหม่ของเส้นเลือดจำเป็นต้องถูกยับยั้ง บทความด้านล่างนี้ตัดตอนและเรียบเรียงมาจากบทคัดย่อของรายงานที่พิสูจน์สรรพคุณของมาโคลิปินในการยับยั้งการสร้างเส้นเลือดใหม่จากการทดลองจริง พร้อมคำอธิบายแบบเข้าใจง่ายเพิ่มเติม
สารสกัดด้วยเอทานอลจากกล้ามเนื้อของปลาฉลาม มีความสามารถในการยับยั้งกระบวนการสร้างเส้นเลือดใหม่ ในการทดลองในห้องปฏิบัติการโดยสถาบันวิจัย ได้มีการเตรียมลิปิดที่สกัดจากปลาฉลาม (มาโคลิปิน) ซึ่งอุดมไปด้วยกรดไขมันไม่อิ่มตัว ซึ่งรวมถึงกรดไขมันโอเมก้า 3 อย่างเช่น กรดโดโคซาเฮกซาอีโนอิก (Docosahexaenoic acid) หรือ DHA จากการทดลองพบว่ามาโคลิปินปริมาณ 5μg/ml สามารถยับยั้งการสร้างเส้นเลือดใหม่ได้ถึง 50% ในการทดลองจริงกับสัตว์ทดลองโดยการให้มาโคลิปินทางปาก พบว่าการสร้างเส้นเลือดใหม่ลดลง 50% เมื่อให้มาโคลิปินในปริมาณ 17mg ต่อน้ำหนักตัว 1 kg นอกจากนี้เมื่อนำมาโคลิปินผสมกับน้ำมันมะกอกที่อัตราส่วน 1:9 พบว่ามีประสิทธิภาพเป็น 2 เท่าในหลอดทดลอง ทั้งนี้ น้ำมันมะกอกเพียงอย่างเดียวไม่พบว่ามีฤทธิ์ในการยับยั้งทั้งในเอออร์ติกริง (Aotic ring) และในหลอดทดลอง
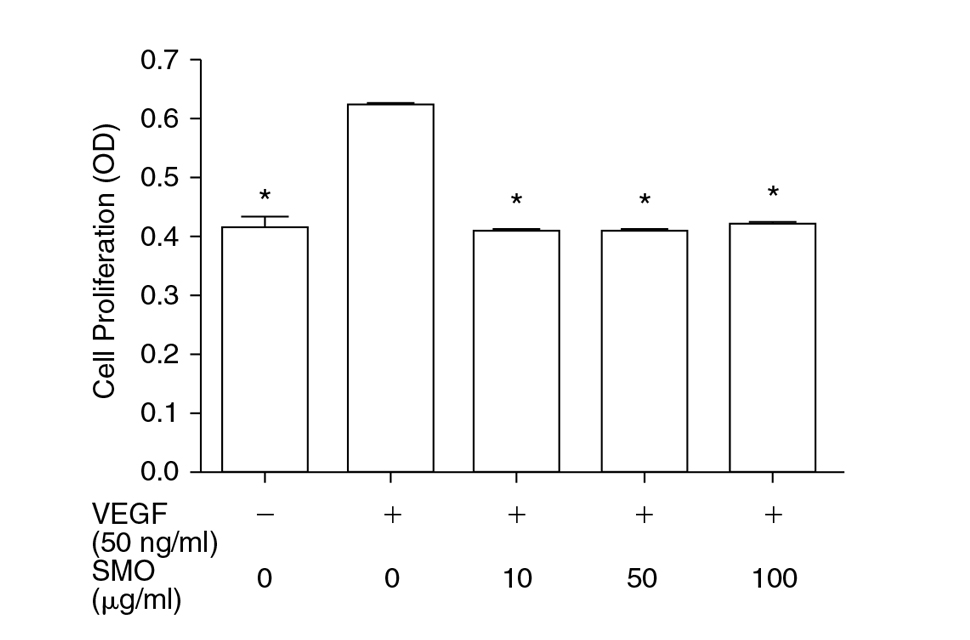
การทดลองนี้ชี้ให้เห็นว่าการจับคู่กันของมาโคลิปินกับน้ำมันมะกอกสามารถลบล้างผลกระทบของปัจจัยกระตุ้นการสร้างเส้นเลือดใหม่ เช่น VEGF, FGF-2 และ TGF-β ซึ่งสารเหล่านี้เป็นปัจจัยการเจริญเติบโตที่กระตุ้นให้เนื้องอกไปเชื่อมตัวกับเส้นเลือดหลักอันจะส่งผลให้เนื้องอกโตและแพร่กระจาย จากการทดลองยังบ่งชี้ให้เห็นว่าส่วนผสมระหว่างมาโคลิปินกับน้ำมันมะกอกที่ 1:9 เป็นสัดส่วนของผลิตภัณฑ์จากธรรมชาติที่รับประทาน มีฤทธิ์ในการรักษาอาการของโรคให้ดีขึ้นและมีฤทธิ์ในการยับยั้งการสร้างเส้นเลือดใหม่ได้อย่างยอดเยี่ยม กลไกการยับยั้งการสร้างเส้นเลือดใหม่ของมาโคลิปินคือการไปยับยั้งการจับตัวกันของ VEGF กับตัวรับสัญญาณ (VEGFR-2 และ VEGFR-1) และยับยั้งการเติมหมู่ฟอสเฟตลงในไทโรซีนของตัวรับสัญญาณ VEGF บนเส้นทางส่งสัญญาณหรืออาจกล่าวอย่างง่ายๆคือ จากการยับยั้งไม่ให้ปัจจัยการเจริญเติบโตไปเกาะติดกับเส้นเลือดจะสามารถเข้าไปขัดขวางการส่งสัญญาณเริ่มสร้างเส้นเลือดใหม่ซึ่งเป็นขั้นตอนถัดไปได้
จากผลการทดลองได้ชี้ให้เห็นว่า มาโคลิปินซึ่งเป็นลิปิดที่มีเอกลักษณ์เฉพาะตัวสกัดได้มาจากเนื้อปลาฉลามบางสายพันธุ์ เป็นผลิตภัณฑ์ทางธรรมชาติที่สามารถบริโภคทางปากได้และมีคุณค่าในฐานะที่เป็นสารยับยั้งการสร้างเส้นเลือดใหม่ มาโคลิปินผ่านการทดสอบด้านความปลอดภัยซึ่งดำเนินการโดยสถาบันทามะ ซึ่งเป็นศูนย์วิจัยด้านอาหารแห่งประเทศญี่ปุ่นพบว่าไม่เป็นพิษและไม่มีสารทำให้เกิดการผิดปกติของพัฒนาการทางร่างกายของทารกตั้งแต่อยู่ในครรภ์มารดา